副标题:Cu/光共催化溴代芳香烃的三氟甲基化
提起偶联反应,人们往往会想到金属Pd催化剂,似乎二者已经成为一个不可分割的整体。事实上,最先用于偶联反应的金属是铜(Cu)。早在1901年,德国化学家Fritz Ullmann就发现芳基卤化物与铜粉共热可生成联芳香烃类化合物;1903年,Ullmann又报道了类似条件下卤代芳香烃的C-N键偶联反应。随后,人们发现这类反应可以广泛地应用于芳基碳-碳、芳基碳-氮、芳基碳-氧、芳基碳-硫键等化学键的形成反应,并将其称为Ullmann缩合反应或Ullmann交叉偶联反应。早期的Ullmann反应存在很大的局限性,如反应条件苛刻、反应时间长、后处理繁琐、收率低、官能团兼容性差等。尽管如此,由于铜催化剂廉价易得,并且一直以来都缺乏有效的手段实现卤代芳香烃和亲核试剂的偶联,Ullmann反应仍被合成工作者广泛使用。20世纪70年代以后,化学家们发现Pd和Ni能够更好地实现这一类型的偶联反应,传统Ullmann反应的研究也逐渐被放弃。然而,经过多年对Pd和Ni催化偶联反应的深入研究,化学家们也发现Pd和Ni催化剂的诸多不足,如Pd催化剂毒性较大、价格昂贵、依赖于不稳定且剧毒的有机膦配体,Ni催化剂毒性大等。为了寻找廉价且低毒性的催化剂,化学家们又将目光重新转移到Cu催化的Ullmann反应。在传统Ullmann反应的复兴之路上,Buchwald、Hartwig、马大为等人做出了开创性的工作,他们以铜盐作为催化剂,使用合适的配体、碱和溶剂等,Ullmann反应不仅能在相对温和的条件和较低负载量催化剂的条件下进行,底物的适用范围及官能团兼容性也得到大幅度提高,激发了人们发展Ullmann反应的浓厚兴趣,越来越多的研究开始集中于改进这一反应的条件,迎来了“Ullmann化学新时代”。为了满足工业化需求,近年来,如何让铜盐催化的Ullmann反应在无配体参与、更温和的条件下进行引起了化学家的广泛关注,但是其进展也十分缓慢,问题究竟出在哪里呢?
目前人们普遍认为,铜盐催化的Ullmann反应经历了Cu(I)-Cu(III)机理:催化剂Cu(I)X首先与亲核试剂HNu作用生成Cu(I)Nu中间体I,然后中间体I与卤代芳香烃Ar-X发生氧化加成反应得到Cu(III)中间体II,中间体II发生还原消除反应得到目标产物,并释放Cu(I)催化剂进入下一个催化循环。化学计量的金属实验研究表明,相比于Pd和Ni,高价Cu通过还原消除反应生成Ar-N、Ar-O、Ar-F和Ar-CF3要容易得多,但是低价Cu的氧化加成反应却要比前两种金属缓慢得多,这一过程也是Cu催化Ullmann反应的决速步骤。为了降低Cu氧化加成过程的能垒,使用合适的配体、较高的温度或是活泼的底物(碘代芳香烃、活化的溴代芳香烃)看似不可避免。当然,也有化学家利用Cu(I)Nu与其他芳基供体,如芳基硼酸等的转金属途径替代其与卤代芳香烃的氧化加成,但是芳基硼酸仍需从卤代芳香烃合成。
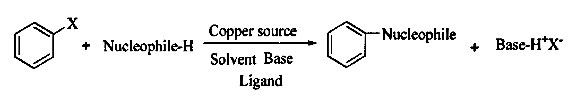
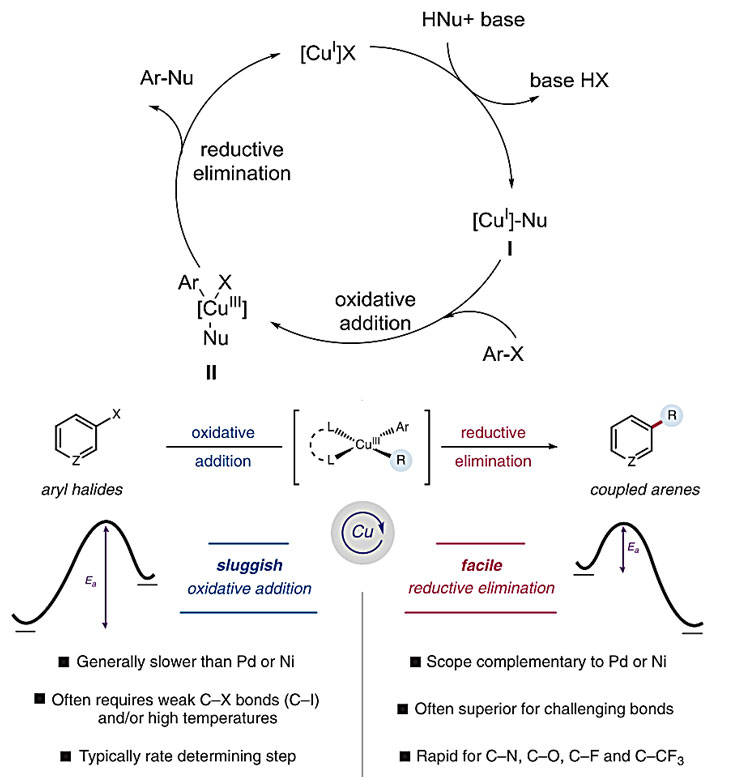
图1. Cu催化Ullmann反应氧化加成-还原消除的机理。图片来源:Science
Cu与Pd最重要的区别在于Cu很容易达到从0到+3的四种氧化态,而Pd通常只能得到0和+2两种稳定的价态。一直以来,Cu的这一特性让Ullmann反应的Cu(I)/Cu(III)-氧化加成-还原消除机理备受争议,有人认为该反应可能经历了Cu(I)/Cu(II)/Cu(III)-自由基机理途径。例如,2012年,Gregory Fu和Jonas Peters等研究者通过设计光诱导化学计量的Cu参与Ullmann C-N键偶联反应证明了自由基机理的可能性(Science, 2012, 338, 647-651),反应条件十分温和(室温甚至-40 ℃)。他们认为在光的激发下,Cu(I)Nu与Ar-X通过单电子转移机制相互作用,生成XCu(II)Nu和Ar自由基,随后XCu(II)Nu捕获Ar自由基形成Cu(III)中间体,三价Cu中间体最后还原消除生成偶联产物。
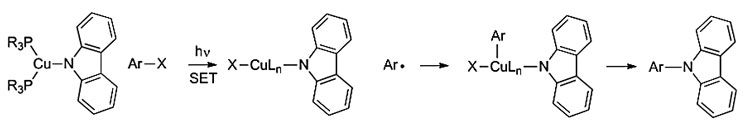
图2. Cu催化Ullmann反应的单电子转移-自由基机理。图片来源:Science
既然化学计量的Cu参与的Ullmann反应可以在温和条件下通过自由基机理进行,那么剩下的问题便是如何在催化条件下诱导芳基自由基产生了。众所周知,Si自由基是有机合成中常用的自由基试剂,由于Si-Br键比C-Br键的键能更高,Si自由基可以攫取溴代物中的Br原子生成亲核性的碳自由基,进而被金属试剂捕获参与偶联反应。2016年,美国普林斯顿大学的David Macmillan教授(点击查看介绍)就利用Si的这一特性成功实现了光/Ni共催化溴代烷烃参与的偶联反应(J. Am. Chem. Soc., 2016, 138, 8084)。进一步的研究表明,Si自由基在光氧化还原体系下同样适用于攫取溴代芳香烃中的卤原子形成芳基自由基。

图3. Si攫取Br生成烷基自由基的策略实现光/Ni共催化的偶联反应。图片来源:J. Am. Chem. Soc.
基于此,最近David Macmillan教授课题组使用以上策略成功实现了光/Cu共催化的溴代芳香烃与CF3亲电试剂间的Ullmann偶联反应。在Ir光敏催化剂和光的作用下,反应通过单电子转移机制,三(三甲基硅基)取代的硅醇4先生成Si自由基,并捕获溴原子形成芳基自由基,而三氟甲基芳基锍盐8则可以生成CF3自由基,两种不同的自由基依次被铜催化剂捕获,历经Cu(I)/Cu(II)/Cu(III)中间体,最终通过还原消除得到芳香烃三氟甲基化的产物。反应中无需使用配体,并能在温和的加热条件下进行。相关工作发表在Science上,共同第一作者为Chip Le、Tiffany Q. Chen和Tao Liang博士。

(从左至右)Chip Le、Tiffany Q. Chen和Tao Liang博士。图片来源:Macmillan Group / Princeton University
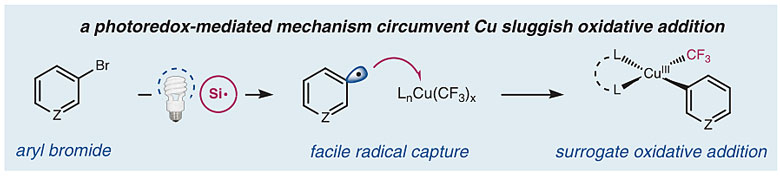
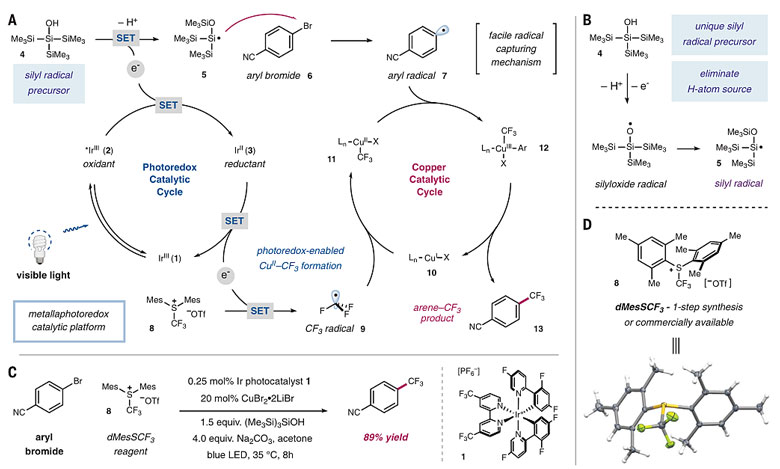
图4. Si攫取Br生成芳基自由基的策略实现光/Cu共催化的偶联反应。图片来源:Science
作者以对位氰基取代的芳基溴和三氟甲基化试剂8作为偶联底物,对反应条件进行了探索,最优条件为使用0.25 mol%的Ir催化剂1、20 mol%的CuBr2•2LiBr、1.5当量的硅醇、4当量的Na2CO3,反应以丙酮作为溶剂,在35 ℃下进行光照,能以89%的产率得到目标产物。底物普适性考察表明,该反应不仅具有良好的官能团兼容性,且适用于各种杂环芳香烃的偶联和多个活性药物分子的后期三氟甲基化修饰。
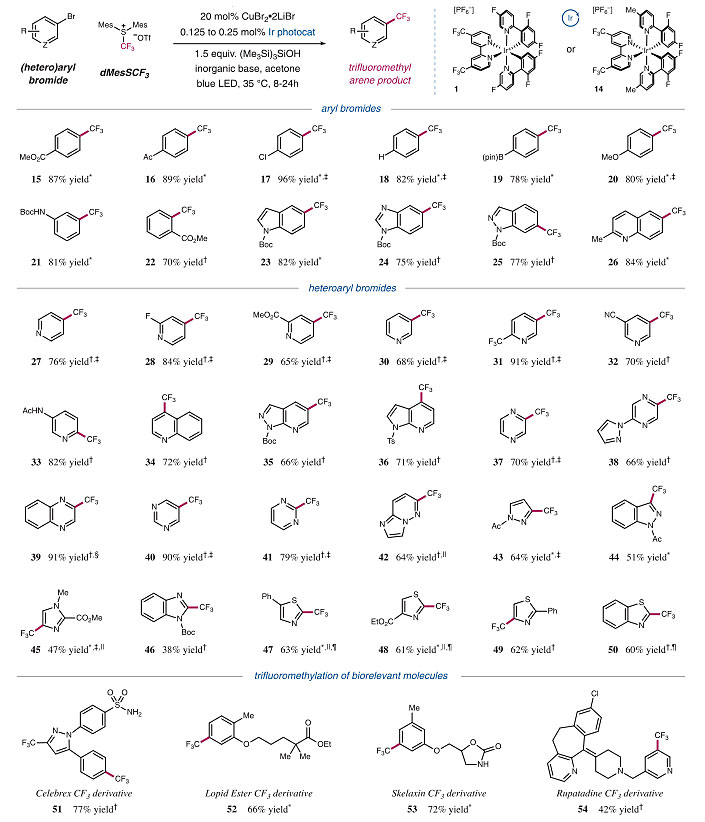
图5. 底物普适性的考察。图片来源:Science
在不加入Cu催化剂的情况下,硅醇诱导生成的芳基自由基可以被H原子、D原子和TEMPO捕获;在标准条件下,三氟甲基化反应亦可被TEMPO试剂淬灭;自由基钟实验可以生成环化产物。这些结果都表明该反应可能通过自由基的机理进行。
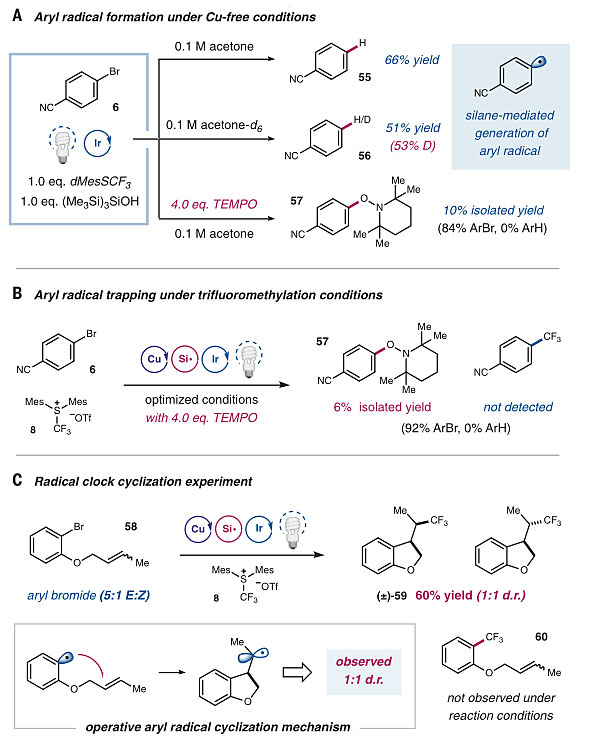
图6. 自由基机理的验证。图片来源:Science
总结
David Macmillan教授发展了一种全新的途径来实现温和条件、无配体参与下的铜催化Ullmann偶联反应。该方法利用光氧化还原反应促使硅醇试剂诱导芳基自由基产生,通过芳基自由基捕获机理克服了铜催化Ullmann偶联反应中氧化加成缓慢的难题。这一策略成功应用于溴代芳香烃的三氟甲基化反应,并将掀起相应模式下新一轮的Ullmann反应研究热潮。
本文版权属于 X-MOL